Liberación de fármacos de una jaula supramolecular
"El truco especial de nuestro sistema son los puntos de ruptura predeterminados"
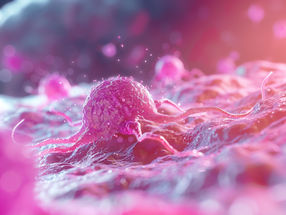
¿Cómo se puede transportar un fármaco muy eficaz al lugar preciso del cuerpo donde se necesita? En la revista Angewandte Chemie, químicos de la Universidad Heinrich Heine de Düsseldorf (HHU), junto con sus colegas de Aquisgrán, presentan una solución mediante una jaula molecular que se abre por ultrasonidos.
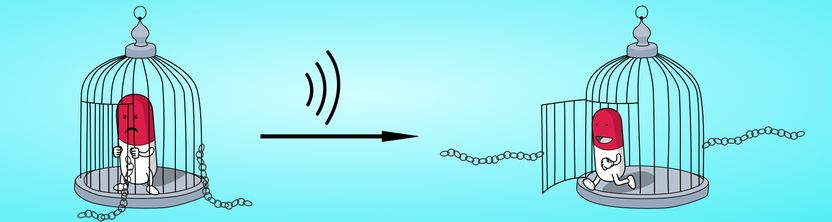
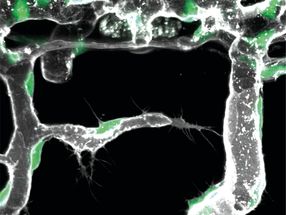
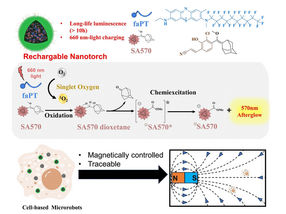
Los investigadores consiguen construir una jaula supramolecular y cargarla con una carga farmacéuticamente activa. En solución acuosa, las ondas ultrasónicas abren la jaula y liberan el fármaco.
HHU / Robin Küng
La química supramolecular consiste en la organización de moléculas en estructuras más grandes y de mayor orden. Cuando se eligen los bloques de construcción adecuados, estos sistemas se "autoensamblan" a partir de sus componentes individuales.
Algunos compuestos supramoleculares se prestan a la "química huésped". En estos casos, una estructura anfitriona encierra a una molécula huésped y puede protegerla y transportarla lejos de su entorno. Este es un campo de especialización del Dr. Bernd M. Schmidt y su grupo de investigación en el Instituto de Química Orgánica y Macromolecular de la HHU.
Los químicos de Düsseldorf colaboraron con sus colegas del Instituto DWI de Materiales Interactivos para encontrar un sistema que algún día pueda incluso transportar moléculas de carga a través del cuerpo humano y liberar el fármaco en el lugar deseado.
La solución puede ser utilizar "jaulas de Pd6(TPT)4" discretas. Se trata de conjuntos octaédricos en forma de jaula, con cadenas de polímero en cada vértice. Se componen de cuatro paneles triangulares, átomos de paladio y unidades de conexión.
Cuando los componentes individuales se añaden a una solución acuosa en la proporción correcta, las jaulas se autoensamblan. Si se añaden moléculas hidrofóbicas más pequeñas a las jaulas, éstas entran en las cavidades. Los investigadores demostraron este efecto utilizando moléculas farmacéuticamente activas, como el ibuprofeno y la progesterona.
"El truco especial de nuestro sistema consiste en los puntos de ruptura predeterminados", explica el Dr. Schmidt, último autor del estudio. "Los átomos de paladio sujetan todos los compuestos con un enlace comparativamente débil. Una vez que se consigue romper los átomos del compuesto, toda la estructura octoédrica se rompe".
Para romper los enlaces, los investigadores de Aquisgrán utilizan una potente ultrasonificación similar a la que se utiliza en medicina para romper los cálculos renales, por ejemplo. En el agua, los ultrasonidos crean burbujas de cavitación que estallan y ejercen una enorme fuerza mecánica de cizallamiento sobre las largas cadenas de polímeros. Las fuerzas son tan potentes que los átomos de paladio se desprenden de los vértices y rompen la jaula octaédrica. Las pequeñas moléculas del fármaco se agitan en el proceso, pero no resultan dañadas.
El Dr. Robert Göstl (DWI) afirma: "La radiación ultrasónica localizada del tejido a tratar podría significar que el fármaco transportado en la jaula se libere posteriormente en el lugar exacto donde se necesita la terapia". Las moléculas de fármacos utilizadas en el estudio sirven sólo de ejemplo. En principio, en la jaula pueden introducirse un gran número de moléculas hidrofóbicas diferentes. A diferencia de otros sistemas huésped descritos, no es necesario alterar químicamente las moléculas de los fármacos para que entren en la jaula. "Para tratar tumores, sería factible utilizar fármacos citostáticos como carga, por ejemplo. Al liberarlos directamente en el lugar de un tumor sólido, podría ser posible una quimioterapia que utilizara mucha menos cantidad del fármaco y, por tanto, tuviera menos efectos secundarios", explica Schmidt.
A ello contribuye el hecho de que el volumen de carga definido permite medir con precisión la cantidad de fármaco que se libera en el lugar de destino. "La dosis administrada podría incluso calcularse con precisión".
El estudio es una prueba de concepto que demostró la viabilidad del método. También convenció a los revisores y editores de la revista "Angewandte Chemie", que calificaron la publicación de muy importante. El trabajo, clasificado como "Hot Paper", también aparecerá en la portada del próximo número.
"Los próximos pasos consisten en determinar cómo responden las células reales a nuestras jaulas. Antes de cualquier uso médico, tenemos que asegurarnos de que no son tóxicas".
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.