La fuente de rayos X de DESY, PETRA III, señala posibles formas de mejorar las vacunas de ARN
La compañía farmacéutica BioNTech y la Universidad de Mainz están llevando a cabo una investigación con otros socios en la línea de tiro del EMBL
La empresa biotecnológica BioNTech, con sede en Maguncia, que recientemente presentó los primeros resultados prometedores de una vacuna contra el coronavirus junto con la empresa estadounidense Pfizer, ya está llevando a cabo una investigación sobre la próxima generación de fármacos ARN en la fuente de rayos X de DESY, PETRA III. Utilizando la línea de haz P12, operada por el Laboratorio Europeo de Biología Molecular EMBL, BioNTech ha estado investigando, junto con las Universidades de Mainz, Tel Aviv y Leiden, así como el Centro de Investigación Jülich y el EMBL, cómo el llamado ARN mensajero (ARNm) puede ser mejor empaquetado para ser más efectivo en el organismo objetivo. Los investigadores informan de varios resultados en tres documentos, publicados en las revistas Applied Nano Materials, Cells y Langmuir. Los documentos también ilustran el potencial de la investigación analítica llevada a cabo con la ayuda de la infraestructura de investigación disponible en el campus de DESY.
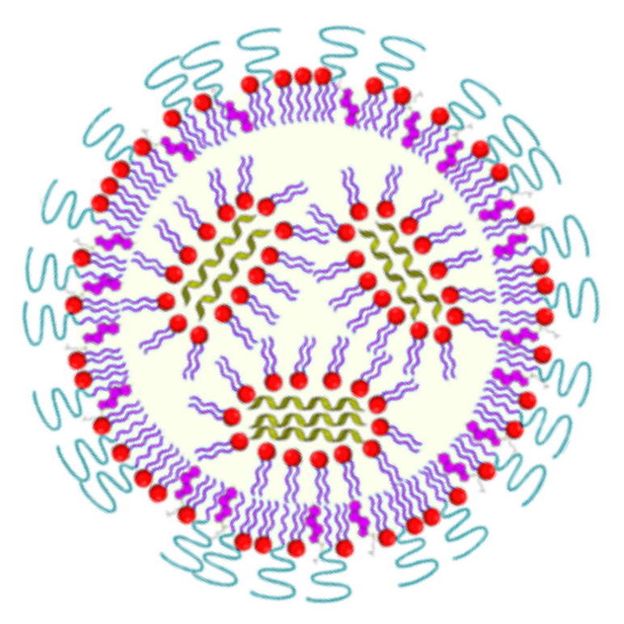
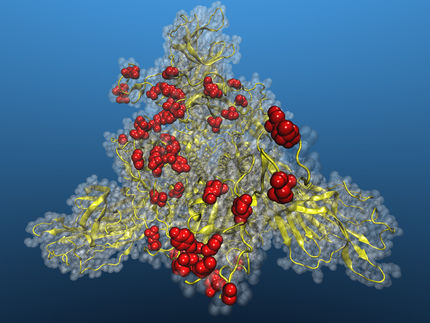
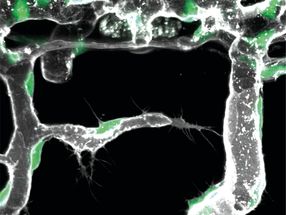
Representación esquemática de una nanopartícula lipídica cargada con ARNm (verde).
BioNTech, Cristina Sala
La vacuna candidata desarrollada por BioNTech y Pfizer, al igual que la potencial vacuna presentada recientemente por la empresa estadounidense Moderna, pertenece a la nueva clase de vacunas de ARNm, que se cree que tienen un gran potencial no sólo para combatir virus sino también para tratamientos personalizados contra el cáncer. Esta nueva técnica consiste en introducir el proyecto de una proteína clave en un patógeno, el llamado antígeno, en las células del sujeto en forma de ARNm, con lo que las células comienzan a producir esta proteína clave. La proteína en sí no causa ninguna enfermedad, pero el sistema inmunológico del cuerpo la reconoce como extraña y comienza a producir anticuerpos contra ella. Si el cuerpo se encuentra más tarde con el patógeno real, el sistema inmunológico reconoce la proteína y ya está preparado.
Este método es muy versátil, permitiendo una rápida respuesta al brote de una epidemia. También es posible hacer que el cuerpo produzca antígenos para ciertas células cancerosas, desencadenando así una respuesta inmunológica a estas células cancerosas. En principio, el plano de cualquier proteína puede introducirse en el cuerpo: no sólo el de un patógeno o una célula cancerosa, sino también las instrucciones para construir proteínas que puedan ayudar a tratar ciertas enfermedades. Estas instrucciones suelen estar codificadas en forma de ARN mensajero. Normalmente, el código del ARNm se lee desde el genoma de ADN dentro de la célula y se convierte en proteínas por las fábricas de proteínas de la célula, los ribosomas. En el caso de una vacuna de ARN, el ARNm preparado se introduce en las células desde el exterior y es procesado directamente por el ribosoma. El material genético propio de la célula, almacenado en el núcleo, permanece inalterado y el ARNm introducido se degrada rápidamente, de modo que la producción de la proteína del patógeno pronto se detiene.
Sin embargo, la introducción del ARNm en la célula es un gran desafío. El ARNm puro sería degradado por las enzimas que se encuentran en todo el tejido incluso antes de que las células pudieran absorberlo. Por lo tanto, se utilizan varias estrategias para ocultar el ARN mensajero dentro de las nanopartículas y así transportarlo dentro de las células del cuerpo. Por regla general, el ARNm se introduce utilizando nanopartículas hechas de ciertos polímeros o los llamados lípidos, las moléculas que forman las membranas celulares, por ejemplo.
Si se configuran adecuadamente, las nanopartículas resultantes son absorbidas por las células, donde se libera el ARNm. La eficiencia de este llamado proceso de transfección es crucial para la eficacia de una vacuna de ARN. En PETRA III, los científicos han estado investigando varios enfoques nuevos para el envasado y la entrega del ARNm.
Entre otras cosas, los científicos han desarrollado nanopartículas lipídicas de ARNm (LNPs) que están hechas a medida para este propósito, utilizando un polímero hecho del aminoácido sarcosina, que es producido naturalmente por el cuerpo. Normalmente, el polietilenglicol (PEG), un polímero ampliamente utilizado en las industrias farmacéuticas y cosméticas, se utiliza para este propósito; pero tiene varias desventajas. El nuevo tipo de PEG condujo a una fuerte producción de la proteína deseada y al mismo tiempo redujo las respuestas inmunológicas no deseadas, como el equipo informa ahora en Applied Nano Materials.
Los investigadores utilizaron la dispersión de rayos X de ángulo pequeño (SAXS) en la línea de haz P12 del EMBL en PETRA III para investigar la organización interna de estas nanopartículas lipídicas y compararon su eficacia en diferentes órganos. De esta manera, esperan identificar aquellas propiedades de los LNP que son cruciales para la captación de ARN por células específicas. Esto proporcionará información esencial para desarrollar partículas a medida para aplicaciones médicas específicas.
Los científicos también utilizaron otros sistemas de modelos lipídicos para investigar cómo la estructura interna de los LNPs reacciona a diferentes valores de pH. Esto es importante porque los cambios en el pH juegan un papel clave en un paso crucial en la absorción de las partículas y su liberación en la célula. Por eso se utilizan los llamados lípidos ionizables para fabricar los LNP, cuya carga cambia en función del pH. Se cree que ajustar el pH exacto al que cambia la carga es una base esencial para la alta eficacia de los LNPs.
Hasta ahora, sólo ha sido posible estudiar esos cambios que dependen del nivel de pH de forma indirecta, por ejemplo, mediante métodos espectroscópicos. El equipo ha logrado por primera vez demostrar directamente los cambios en la estructura de las membranas modelo que contienen los lípidos ionizables. La investigación publicada en la revista Langmuir describe cómo el pH influye en la estructura interna de las nanopartículas. Este conocimiento puede utilizarse para desarrollar sistemas de transporte optimizados para la transferencia de tipos específicos de células, ya que el pH varía de un tipo de célula a otro.
La eficiencia de la transfección de ARNm también puede aumentarse utilizando la combinación adecuada de diferentes materiales para fabricar las nanopartículas, como se demostró en otro proyecto de investigación. Como escriben los científicos involucrados en la revista Cells, las nanopartículas híbridas, que contienen tanto lípidos como polímeros convenientemente combinados, lograron una transfección significativamente mejor que las nanopartículas de lípidos puros o de polímeros puros. Los análisis estructurales, algunos de los cuales se llevaron a cabo en la línea de haz P12 del EMBL en PETRA III, muestran que las partículas con mayor eficiencia de transfección se caracterizan por una estructura interna heterogénea en la que se alternan áreas bien ordenadas y otras menos ordenadas en un patrón característico. Por lo tanto, muestran una cierta similitud con los materiales compuestos estudiados por los científicos de materiales.
Los tres enfoques ofrecen oportunidades para lograr una mejor comprensión de los principios fundamentales que rigen la eficacia de los medicamentos basados en el ARNm y, por consiguiente, para seguir mejorando las futuras vacunas de ARNm y optimizarlas individualmente para aplicaciones específicas. La transformación es un aspecto decisivo para el éxito de las vacunas de ARNm, en el que actualmente se depositan grandes esperanzas. Además de BioNTech, Pfizer y Moderna, otras empresas como Curevac, con sede en Tubinga, también están trabajando en vacunas de coronavirus basadas en ARNm. Aunque todavía hay que investigar otros aspectos, como la eficacia a largo plazo, esto ya da una idea del potencial que ofrece esta tecnología, que en principio podría utilizarse para desarrollar muy rápidamente vacunas contra una serie de enfermedades infecciosas, pero también vacunas terapéuticas para el tratamiento de enfermedades existentes como el cáncer.
La investigación muestra las extraordinarias oportunidades de investigación y experimentación que están disponibles a través de la infraestructura de investigación en el campus del DESY, permitiendo que se avance en la innovación, la tecnología y la medicina. En tiempos de crisis, como la actual pandemia de coronavirus, la investigación analítica en particular es enormemente relevante. Tales análisis pueden conducir a importantes hallazgos que pueden ser utilizados para desarrollar nuevos ingredientes farmacéuticos activos. Su potencial está lejos de haberse agotado.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
"Hybrid Biopolymer and Lipid Nanoparticles with Improved Transfection Efficacy for mRNA"; Christian D. Siewert, Heinrich Haas, Vera Cornet, Sara S. Nogueira, Thomas Nawroth, Lukas Uebbing, Antje Ziller, Jozef Al-Gousous, Aurel Radulescu, Martin A. Schroer, Clement E. Blanchet, Dmitri I. Svergun, Markus P. Radsak, Ugur Sahin and Peter Langguth; Cells; 2020.
"Polysarcosine-Functionalized Lipid Nanoparticles for Therapeutic mRNA Delivery"; Sara S. Nogueira, Anne Schlegel, Konrad Maxeiner, Benjamin Weber, Matthias Barz, Martin A. Schroer, Clement E. Blanchet, Dmitri I. Svergun, Srinivas Ramishetti, Dan Peer, Peter Langguth, Ugur Sahin, and Heinrich Haas; Applied Nano Materials; 2020.
"Investigation of pH-Responsiveness inside Lipid Nanoparticles for Parenteral mRNA Application Using Small-Angle X‐ray Scattering"; Lukas Uebbing, Antje Ziller, Christian Siewert, Martin A. Schroer, Clement E. Blanchet, Dmitri I. Svergun, Srinivas Ramishetti, Dan Peer, Ugur Sahin, Heinrich Haas, and Peter Langguth; Langmuir; 2020.