Die Vermessung des Unmessbaren
Mehrere hundert Zellen simultan erfassen und auswerten
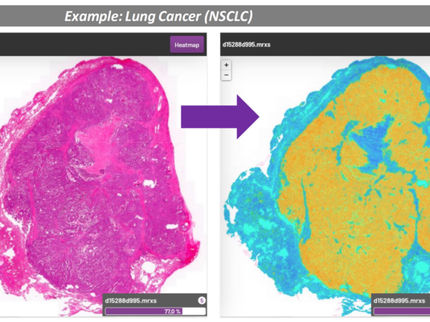
Wissenschaftler des Leibniz-Instituts für Pflanzenbiochemie haben gemeinsam mit Partnern der Martin-Luther-Universität Halle-Wittenberg ein Programm entwickelt, mit dem es möglich ist, die Form und Größe von Pflanzenzellen zu vermessen. Das Programm mit dem Namen PaCeQuant (von Pavement Cell Quantification) erfasst automatisch spezifische Parameter von mehreren hundert Blattepidermis-Zellen gleichzeitig. Es baut auf bereits genutzte Bildanalyseprogramme auf und ist als OpenSource-Software für jedermann frei verfügbar.

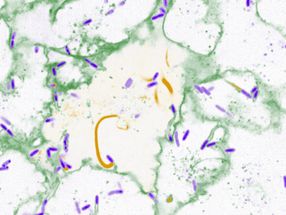
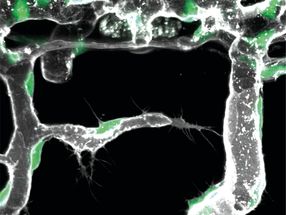
Einteilung von Arabidopsis-Blattepidermis-Zellen in klein, mittelgroß und groß; jeweils 3, 5 und 7 Tage nach der Keimung (Days after Germination, DAG) durch PaCeQuant.
Katharina Bürstenbinder, IPB
Wie vermisst man die Welt, die nicht messbar ist? Vor dieser Frage und Herausforderung stand Katharina Bürstenbinder vom Leibniz-Institut für Pflanzenbiochemie vor etwa zwei Jahren im Rahmen ihrer Forschungsarbeiten. Die promovierte Biologin untersucht Proteine, die den Auf- und Abbau des Zytoskeletts beeinflussen. Das Zytoskelett durchzieht wie ein Netz aus inneren Halteseilen jede Zelle und bestimmt somit deren Größe, Form und Stabilität. Wächst die Zelle in die Länge, verändert sich vorher ihr Zytoskelett. Auf der Suche nach Faktoren, die das feine Zusammenspiel von Zellwachstum und Zellformung regulieren, analysierten die Hallenser Wissenschaftler Blattepidermis-Zellen der Ackerschmalwand Arabidopsis thaliana.
Dabei konnten sie verschiedene Mutanten herstellen, bei denen das Zytoskelett und damit die Form der Blattepidermis-Zellen verändert war. Während die Wildtypzellen ihre typische unregelmäßige Puzzleteilchen-Form aufwiesen, waren die Mutantenzellen lang gestreckter und mit weniger Aus- und Einbuchtungen versehen. Bei einigen Mutantenpflanzen war dieser Unterschied in der Zellform sehr klar erkennbar; bei anderen wiederum nicht. Deren Blattepidermis-Zellen wirkten irgendwie anders – aber waren sie das auch? War bei diesen Zellen in der Tat die Anzahl und Größe der Ausbuchtungen verändert oder war das nur ein subjektiver Eindruck?
Ist die Ausstülpung einer Zelle überhaupt mathematisch klar definiert? – fragte sich daraufhin Bürstenbinder. Gibt es Methoden, mit denen man Zellform und -fläche, die Art und Anzahl der Ausstülpungen und Einbuchtungen exakt bestimmen kann? Eine Suche in der Literatur brachte wenig Ergebnisse: „Hier klafft eine große Methoden-Lücke“, fasst Bürstenbinder zusammen. „Bei allen bisher verwendeten Verfahren zur räumlichen Vermessung von Zellen spielt menschliches Ermessen eine große Rolle. Der Mensch aber kann sich irren.“
Bis heute untersuchen Forscher komplizierte Zellformen, indem sie sie einzeln am computervernetzten Mikroskop begutachten. Die Ränder der Zellen werden mühsam per Hand nachgezeichnet; Ausstülpungen und Einbuchtungen werden händisch definiert. „Je nach gewählter Auflösung übersieht man kleinere Ausbuchtungen schnell“, konstatiert die Hallenser Wissenschaftlerin. Am Ende führt ein Bildanalyseprogramm alle erhobenen Daten zusammen. Für statistisch relevante Ergebnisse müssen mehrere hundert Zellen derart unter die Lupe genommen werden. Das Verfahren kostet – trotz Computerhilfe – sehr viel Zeit und ist zudem mit Ungenauigkeiten und Subjektivität behaftet.
Subjektives Empfinden, wie etwas wirkt, steht natürlich den wissenschaftlichen Prinzipien nach Mess- und Reproduzierbarkeit diametral entgegen. Gegebenheiten, die man nicht mit Zahlen erfassen kann, sind schlecht miteinander vergleichbar. Also entwickelte Bürstenbinder gemeinsam mit Birgit Möller und Yvonne Pöschl das Epidermiszellen-Quantifizierungsprogramm PaCeQuant. Pöschl und Möller trugen als Informatikerinnen der Hallenser Universität mit ihrer Expertise erheblich zum Gelingen des Projektes bei. Für die Entwicklung von PaCeQuant haben die Wissenschaftlerinnen 27 verschiedene Parameter festgelegt, die die Form einer Zelle bestimmen und berechenbar machen. Diese Parameter, wie Zellumfang, Anzahl und Größe der Ausstülpungen, Zellfläche mit und ohne Ausstülpungen werden von PaCeQuant anhand von definierten Messpunkten automatisch erkannt und berechnet. Zudem kann das Programm die Daten von mehreren hundert Zellen simultan erfassen und auswerten.
Die Probe auf’s Exempel war spannend: „Wir haben dann die gleichen Zellen jeweils von PaCeQuant und von verschiedenen externen Personen auf herkömmliche Weise vermessen lassen.“ Die Schwankungen beim herkömmlichen Verfahren betrugen bis zu 40 Prozent. Während das Programm für eine Zelle beispielsweise 20 Ausstülpungen berechnet hatte, kamen die menschlichen Experimentatoren auf Zahlen zwischen 12 und 28. „Diese Unterschiede sind nicht nur vom jeweiligen Vermesser abhängig, sondern sogar von dessen Tagesform“, weiß Bürstenbinder.
Die Anwendungsmöglichkeiten von PaCeQuant sind vielfältig. Veränderte Zellformen von verschiedenen Mutantenzellen können jetzt automatisiert und objektiv voneinander und auch von den Wildtypzellformen abgegrenzt werden. Darüber hinaus erkennt das Programm altersbedingte Unterschiede in der Zellform. Nach vorgegebenen Parametern kann es die Zellen in klein, mittelgroß oder groß einteilen. Es erfasst damit die Anzahl und Verteilung von Zellen in unterschiedlichen Entwicklungsstadien. Pflanzenphysiologen können jetzt verschiedene Wachstumsstadien der Pflanze noch feingliedriger einteilen und schärfer voneinander abgrenzen. Zudem kann das Programm auf die Vermessung anderer Zelltypen in anderen Organismen angepasst werden. So wäre beispielsweise die automatische Erkennung von entarteten Zellen in der Krebsdiagnostik mit PaCeQuant denkbar.
Katharina Bürstenbinder hofft, dass das Programm zunächst von möglichst vielen Pflanzenwissenschaftlern genutzt wird. „Gerade wenn verschiedene Arbeitsgruppen am gleichen Zelltyp arbeiten, entsprächen die Bildanalysen mit PaCeQuant einem einheitlichen Standard und können so viel besser miteinander verglichen und diskutiert werden.“ Erste Interessenten gibt es bereits. Mit ihnen wurden erste Optimierungen für eine Anpassung von PaCeQuant auf andere Zelltypen vorgenommen. Die Vorteile des OpenSource-Programmes zeigen sich bereits jetzt: Wissenschaftler aus aller Welt können das Programm gemeinsam und sehr dynamisch an ihre jeweiligen Fragestellungen und Bedürfnisse anpassen.